Hidrokarbon siklik adalah senyawa organik yang terdiri dari atom karbon dan hidrogen yang terikat untuk menyebabkan cincin atau struktur siklik. Ada terutama dari tiga jenis: alisiklik, aromatik dan polisiklik.
Jenis hidrokarbon ini kemudian dapat terdiri dari alkana, alkena, dan alkuna versi tertutup; memiliki cincin dengan sistem aromatik, seperti benzena dan turunannya; atau menyajikan struktur yang rumit dan menarik. Dari semuanya, alisiklik adalah yang paling sederhana, dan biasanya direpresentasikan dengan menggunakan poligon.
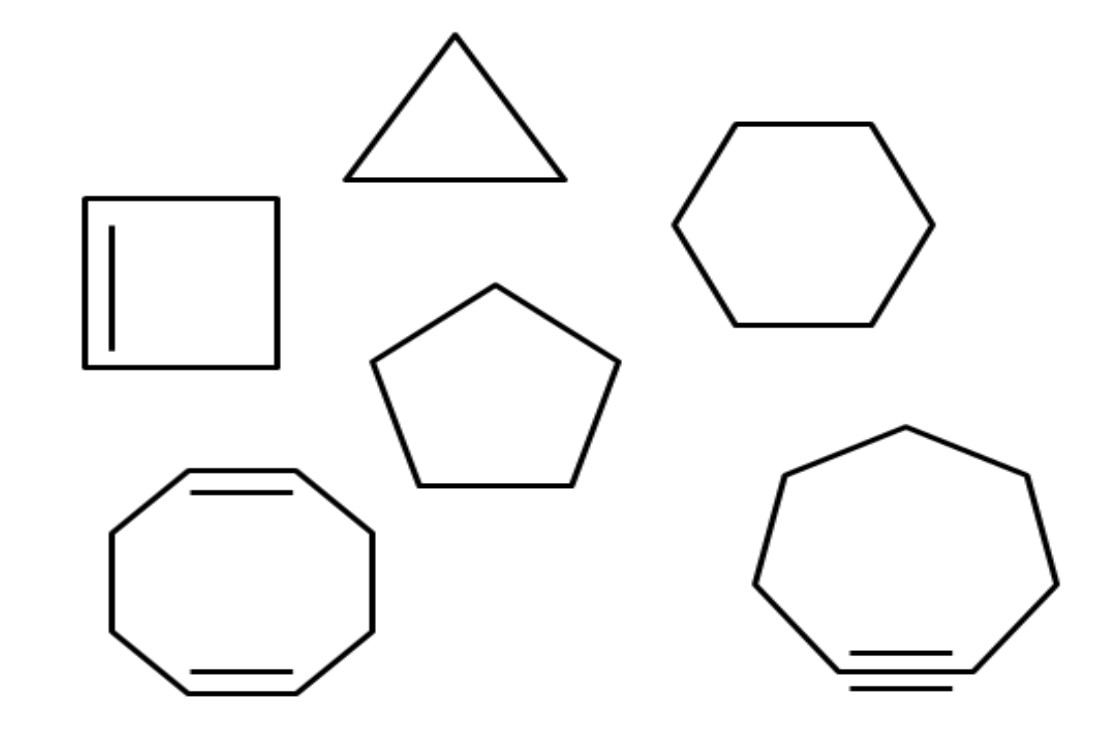
Hidrokarbon alisiklik. Sumber: Gabriel Bolivar.
Di atas misalnya Anda memiliki beberapa hidrokarbon alisiklik. Mereka terlihat seperti poligon sederhana: persegi, segitiga, segi lima, segi enam, dll. Jika salah satu ikatan CC-nya dapat dipotong dengan gunting, hasilnya adalah alkana, alkena (jika memiliki ikatan rangkap) atau alkuna (jika memiliki ikatan rangkap tiga).
Sifatnya tidak terlalu berbeda dari hidrokarbon rantai terbuka asalnya; meskipun, secara kimia, semakin besar ukurannya, semakin stabil, dan interaksinya dengan medium molekuler menjadi lebih jelas (karena area kontaknya lebih besar).
Struktur Hidrokarbon siklik
Langsung ke masalah yang menyangkut struktur mereka, harus diklarifikasi bahwa mereka tidak datar, bahkan ketika dalam representasi poligon mereka tampak begitu. Satu-satunya pengecualian untuk pernyataan ini ditemukan di siklopropana (segitiga), karena ketiga titiknya harus terletak pada bidang yang sama.
Perlu juga dijelaskan bahwa istilah ‘siklus’ dan ‘cincin’ sering kali dapat dipertukarkan; sebuah cincin tidak harus berbentuk lingkaran, dan oleh karena itu cincin itu dapat memperoleh geometri tak berujung selama itu adalah struktur tertutup. Siklopropana kemudian dikatakan memiliki cincin atau siklus segitiga.
Semua karbon memiliki hibridisasi sp 3 , sehingga geometrinya adalah tetrahedral dan ikatannya idealnya dipisahkan dengan sudut 109,5 °; namun, ini tidak mungkin untuk struktur yang tertutup seperti siklopropana, siklobutana (persegi), atau siklopentana (pentagon).
Kita berbicara kemudian dari ketegangan yang mendestabilkan molekul, dan ditentukan secara eksperimen dengan mengukur memanaskan rata-rata pembakaran setiap CH 2 kelompok .
konformasi
Dan apa yang terjadi ketika ada ikatan rangkap dua atau rangkap tiga? Ketegangan meningkat, karena di mana ada salah satunya, struktur akan dipaksa untuk “menyusut” dan tetap datar; yang, secara berurutan, akan memaksa satu konformasi atas yang lain, mungkin gerhana atom hidrogen tetangga.
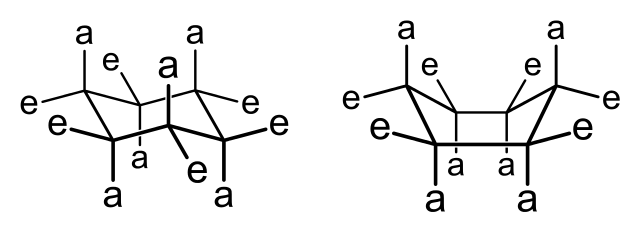
Konformer untuk sikloheksana. Sumber: Sponk [Domain publik]
Pada gambar di atas, dua konformer untuk sikloheksana ditunjukkan untuk mencoba menjelaskan hal di atas. Atom-atom yang berada pada posisi a atau e disebut aksial atau ekuator. Perhatikan bahwa alih-alih segi enam datar, Anda memiliki kursi (kiri) dan perahu (kanan).
Struktur ini dinamis dan membangun keseimbangan di antara mereka. Jika atom dalam a sangat besar, cincin akan “terjepit” untuk memposisikannya pada posisi ekuator; karena di sana mereka berorientasi ke sisi cincin (yang akan memperkuat atau merusak interaksi antarmolekul).
Jika kita melihat masing-masing karbon secara terpisah, akan terlihat bahwa mereka adalah tetrahedral. Ini tidak akan terjadi jika ada ikatan ganda: sp nya 2 hibridisasi akan memaksa struktur untuk meratakan; dan jika ada ikatan rangkap tiga, untuk menyelaraskan. Struktur planar benzena adalah representasi maksimum dari ini.
Sifat Hidrokarbon siklik
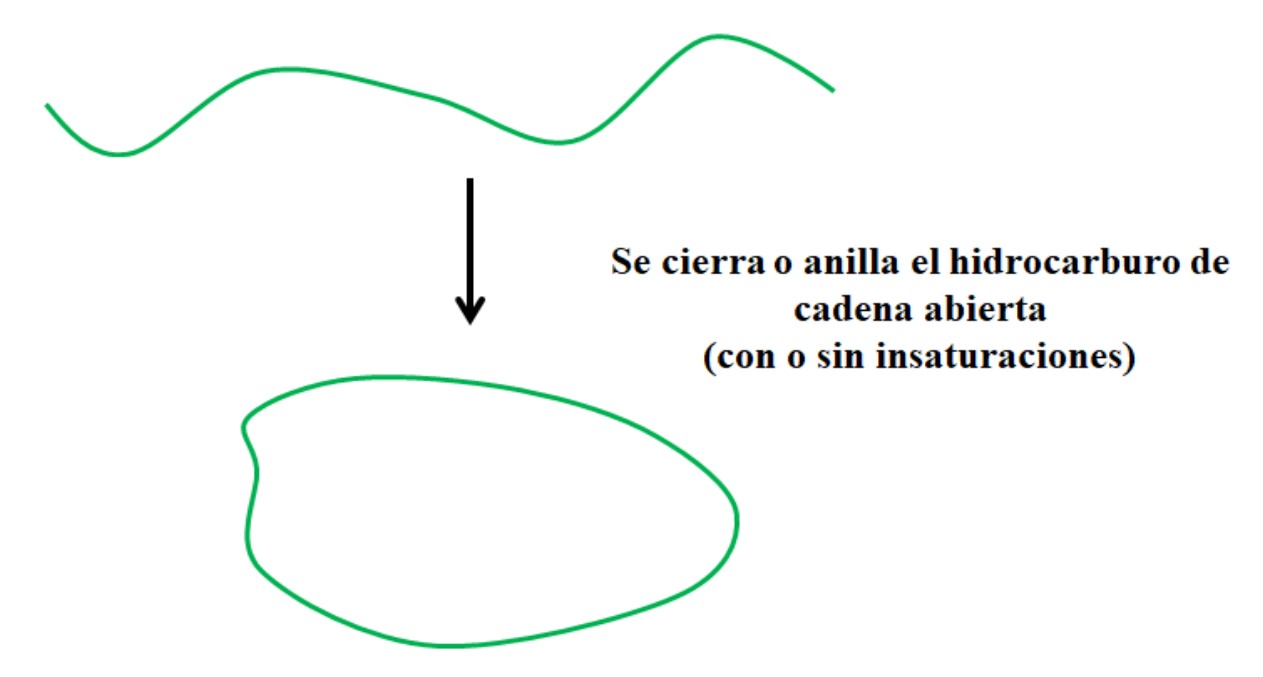
Proses sederhana di mana hidrokarbon siklik terbentuk. Sumber: Gabriel Bolivar.
Misalkan Anda memiliki hidrokarbon rantai terbuka (dengan atau tanpa ketidakjenuhan atau cabang). Jika kita bisa menggabungkan ujungnya, itu akan membuat cincin atau siklus (seperti pada gambar di atas).
Dari sudut pandang sintesis organik, ini tidak terjadi begitu saja; harus ada gugus pergi yang baik yang dihubungkan di ujung rantai, yang ketika keluar, mendorong penutupan rantai (jika larutan sangat encer).
Dengan pemikiran ini, dapat dilihat bahwa hidrokarbon jejak hijau hanya mengalami transformasi sehubungan dengan strukturnya; tanpa memutuskan atau menambahkan ikatan baru dengan atom lain. Artinya secara kimiawi tetap sama sebelum dan sesudah penutupan atau girdling.
Oleh karena itu, sifat kimia atau fisik dari hidrokarbon alisiklik ini tidak terlalu berbeda dari rekan-rekan rantai terbuka mereka. Keduanya reaktif terhadap spesies yang sama (yaitu halogen di bawah sinar ultraviolet), dan dapat mengalami oksidasi kuat atau terbakar dengan melepaskan panas.
Gaya antarmolekul
Ada fakta yang tidak dapat disangkal: cincin memiliki area kontak yang lebih besar daripada rantai terbuka, dan oleh karena itu interaksi antarmolekulnya lebih kuat.
Hasilnya adalah titik didih dan titik lelehnya cenderung lebih tinggi, begitu pula densitasnya. Karena banyak perbedaan dapat dicatat dalam indeks bias atau tekanan uapnya.
Tata nama Hidrokarbon siklik
Kembali ke contoh hidrokarbon dengan goresan hijau, nomenklaturnya tetap tidak berubah setelah menutup dirinya sendiri (seperti ular yang menggigit ekornya sendiri). Oleh karena itu, aturan penamaan tetap sama; kecuali hidrokarbon polisiklik atau aromatik ditangani.
Tiga senyawa ditunjukkan di bawah ini, yang akan diberi nama yang tepat:
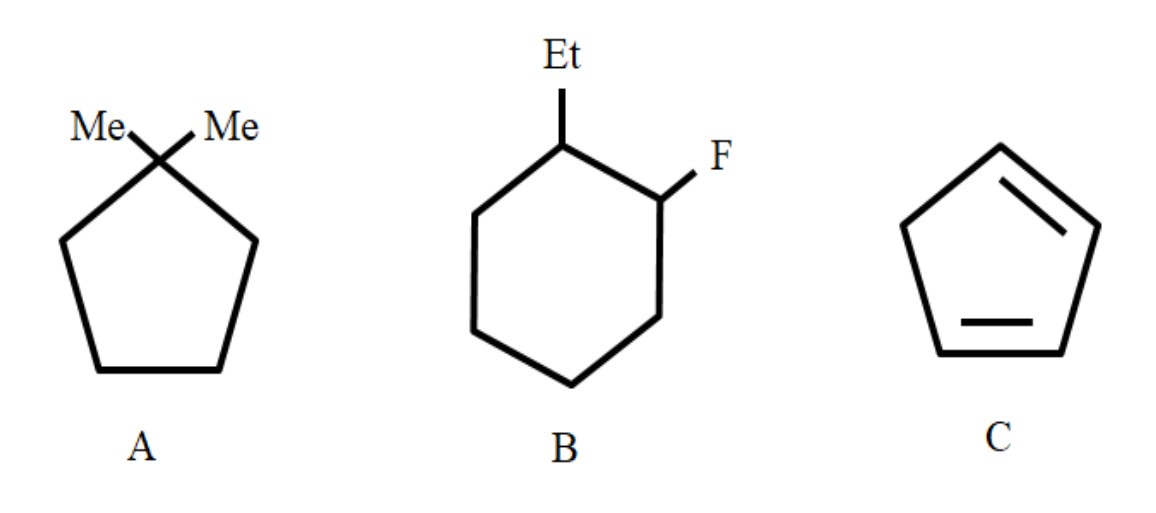
Tiga contoh hidrokarbon siklik untuk menetapkan nomenklaturnya. Sumber: Gabriel Bolivar.
Untuk memulainya, karena mereka adalah struktur tertutup, siklus awalan digunakan untuk merujuknya (di sini kata ring diturunkan).
Dari kiri ke kanan kita memiliki: siklopentana, sikloheksana, dan siklopentana lainnya. Karbon terdaftar sedemikian rupa sehingga substituen diberi nomor terendah, dan selanjutnya disebutkan dalam urutan abjad.
Jadi, A adalah: 1,1-Dimetilsiklopentana. Dalam B kita mulai dengan menyebutkan substituen etil sebelum fluor, jadi namanya adalah: 1-etil-2-fluorosikloheksana. Dan kemudian untuk C, ikatan rangkap diambil sebagai substituen, jumlah karbon yang membentuknya harus ditunjukkan: 1,3-siklopentadiena.
Contoh Hidrokarbon siklik
Sepanjang artikel, disebutkan beberapa hidrokarbon siklik. Pada gambar pertama dapat ditemukan: siklopropana, siklobutana, siklopentana, sikloheksana, sikloheptana dan siklooktan.
Berbagai turunan dapat diperoleh dari mereka, dan cukup untuk menempatkan ikatan rangkap atau rangkap tiga pada mereka untuk masing-masing memiliki sikloalkena atau sikloalkin. Dan sehubungan dengan hidrokarbon aromatik, cukup dengan mengingat cincin benzena dan mengganti atau mereproduksinya dalam dua dimensi.
Namun, yang paling luar biasa (dan bermasalah dalam memahami nomenklaturnya) adalah hidrokarbon polisiklik; artinya, poligon sederhana tidak cukup bahkan untuk merepresentasikannya dengan cara yang sederhana. Tiga di antaranya yang layak disebutkan adalah: Kuba, Canastano dan Pagoda (gambar di bawah).
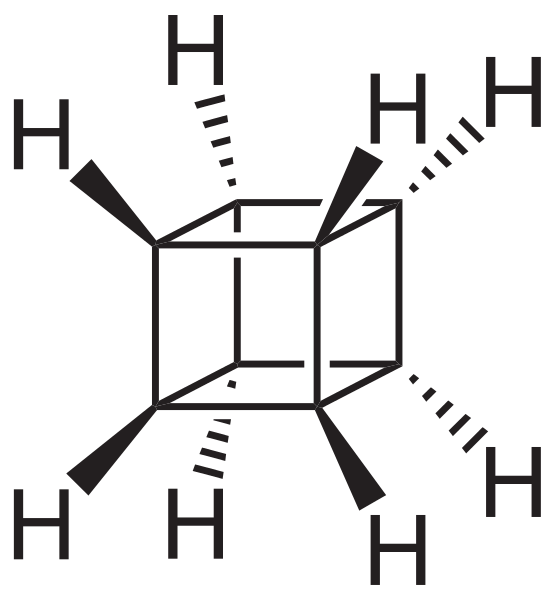
Kerangka Kuba. Sumber: NEUROtiker [Domain publik].
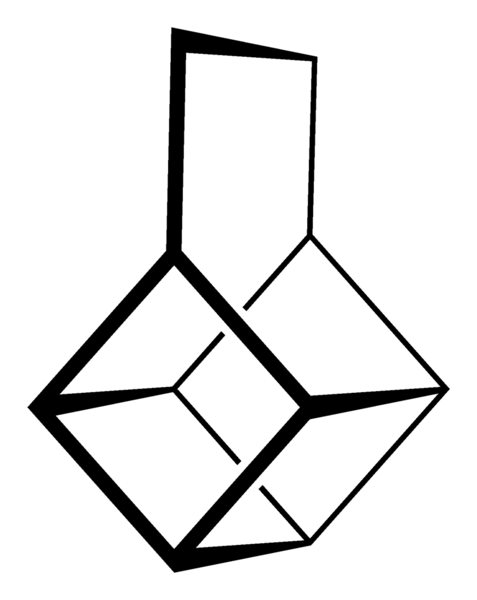
Kerangka canastano. Sumber: Benjah-bmm27 [Domain publik].
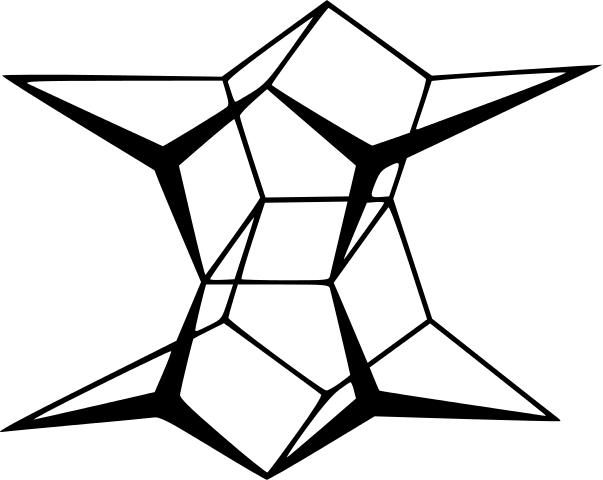
Kerangka pagodano. Sumber: Puppy8800 [Domain publik]
Masing-masing dari mereka memiliki metodologi sintesis yang kompleks, sejarah, seni, dan daya tarik laten untuk kemungkinan struktural tak terbatas yang dapat dicapai oleh hidrokarbon sederhana.
Referensi
- Morrison, RT dan Boyd, R, N. (1987). Kimia organik. Edisi ke-5. Editorial Addison-Wesley Interamericana.
- Carey F. (2008). Kimia organik. (Edisi keenam). Bukit Mc Graw.
- Graham Solomons TW, Craig B. Fryhle. (2011). Kimia organik. amina. (edisi ke-10.). Wiley Plus.
- Reid Danielle. (2019). Hidrokarbon Siklik: Definisi & Contoh. Belajar. Diperoleh dari: study.com
- Yayasan CK-12. (05 Juni 2019). Hidrokarbon siklik. LibreText Kimia. Dipulihkan dari: chem.libretexts.org
- Wikipedia. (2019). senyawa siklik. Dipulihkan dari: en.wikipedia.org
- Koboi Miguel. (2019). Hidrokarbon siklik. Dipulihkan dari: deciencias.net